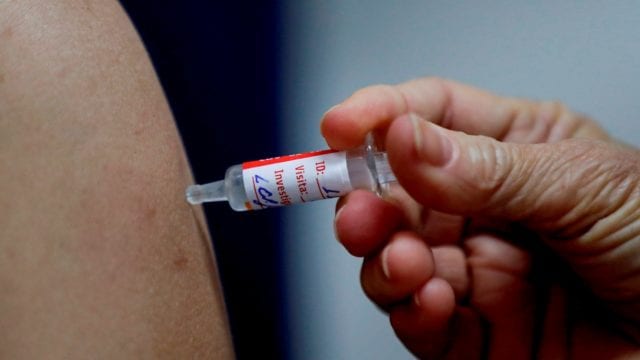
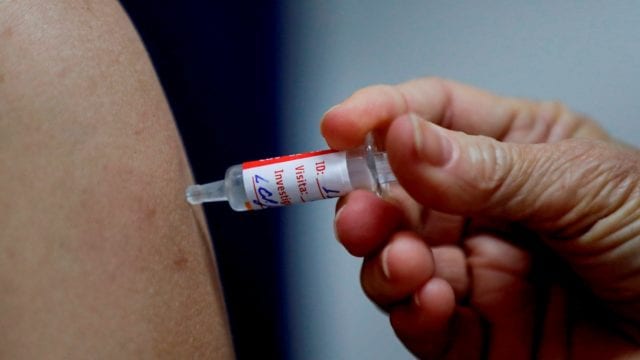
Es por esto que están estancadas las vacunas de AstraZeneca y Johnson & Johnson
Los dos ensayos en pausa hacen resurgir interrogantes sobre los vectores adenovirales, que se han utilizado en experimentos de laboratorio, animales y humanos durante años.
Dos vacunas contra el COVID-19 estancadas por posibles efectos secundarios comparten una característica clave en común: ambas están basadas en adenovirus, gérmenes del resfriado que los investigadores han utilizado en terapias experimentales durante décadas con resultados variables.
Johnson & Johnson dijo el lunes pasado que pausaría su ensayo para investigar una enfermedad, que no especificó, en un participante del estudio. Mientras tanto, el ensayo en Estados Unidos de la vacuna que AstraZeneca está desarrollando con la Universidad de Oxford ha estado suspendido durante más de un mes por decisión de los reguladores después de que surgieran síntomas neurológicos en dos voluntarios.
Con la suspensión de AstraZeneca, las vacunas de Moderna y Pfizer-BioNTech han tomado la delantera en la carrera por ser los primeros en lanzar una vacuna. Mientras tanto, los dos ensayos en pausa hacen resurgir interrogantes sobre los vectores adenovirales, que se han utilizado en experimentos de laboratorio, animales y humanos durante años. En algunos casos, los experimentos han tenido éxito, pero no siempre.
Y este año, cuando las vacunas contra el COVID-19 están entrando fuertemente en la política del momento, la transparencia y la confianza son clave para combatir un virus que ha afectado a más de 39 millones de personas en todo el mundo y ha perjudicado las economías. Si se validan las preocupaciones en torno a los efectos secundarios de las vacunas experimentales en ensayos que utilizan adenovirus, podría aumentar el escepticismo en el público general y plantear preguntas para otros laboratorios farmacéuticos.
“Si bien podría ser una coincidencia”, dijo Sam Fazeli, analista de Bloomberg Intelligence, en una nota de investigación, “aún existe la posibilidad de que las vacunas de vectores adenovirales tengan un mayor riesgo de efectos secundarios escasos –por ejemplo, ataques autoinmunes como mielitis transversa– que las de Pfizer-BioNTech, Moderna o Novavax”.
Las suspensiones para investigar efectos secundarios no son inusuales en los ensayos de vacunas, que exigen un requisito de alta seguridad debido a que se suministran a personas sanas. Oxford ha dicho que no hay pruebas suficientes para conectar las enfermedades de los participantes con su vacuna. Sus pruebas en humanos en el Reino Unido, Sudáfrica y Brasil se reanudaron hace semanas.
Los vectores adenovirales están bien estudiados, son versátiles y se ha demostrado que son bien tolerados, por lo que son buenos candidatos para las vacunas contra el COVID, señaló AstraZeneca en un correo electrónico. Las reacciones a la vacuna de Astra-Oxford en los primeros estudios fueron comparables a las observadas en ensayos anteriores de otras vacunas que usan adenovirus, dijo la compañía. Los investigadores de Oxford declinaron hacer comentarios.
En algunos casos, los experimentos con adenovirus han tenido éxito. A principios de este año, por ejemplo, una vacuna de J&J basada parcialmente en un adenovirus fue aprobada para combatir el ébola, que ha cobrado la vida de miles de personas en África.
En otros experimentos, sin embargo, hubo resultados decepcionantes. En 2008, una vacuna con adenovirus desarrollada por Merck & Co para prevenir el VIH fue vinculada a un aumento de infecciones entre algunos que la recibieron en un ensayo. Merck abandonó la vacuna y varios programas similares quedaron en el camino.
Si los investigadores en los ensayos actuales determinan que la causa de los episodios está relacionada con las vacunas, buscarían posibles vínculos con el enfoque del adenovirus y con la proteína espiga que la vacuna apunta a elaborar para preparar el sistema inmunológico ante una infección real, según Michael Kinch, especialista en vacunas de la Universidad de Washington, en St. Louis.
En este punto, dijo, no hay suficiente información conocida. “¿Es solo casualidad?”, dijo Kinch. “En primer lugar, está la mala suerte. Si resulta que hay una correlación y una causalidad, entonces la conversación cambia muy rápidamente”.
J&J dijo que aún está aprendiendo sobre la enfermedad del participante en su ensayo. El adenovirus en su vacuna experimental contra el COVID se ha utilizado en todo el mundo en más de 110.000 personas, según Paul Stoffels, director científico de la compañía.
Modificación de genes
Descubiertos en las glándulas adenoides humanas en 1953, los adenovirus tienen una serie de características que se prestan para el suministro de medicamentos. Si bien algunos infectan fácilmente las células humanas, solo causan síntomas leves en la mayoría de los casos. Las cepas que aparecen en diferentes animales, como vacas y chimpancés, se pueden adaptar a diferentes propósitos, como vacunas veterinarias.
Y lo mejor de todo es que a los científicos les ha resultado relativamente fácil mezclar y combinar genes dentro de ellos, ofreciendo una variedad de características y propiedades.
“Se eliminan los genes que controlan la capacidad del virus para proliferar”, dijo Ron Crystal, investigador de Weill Cornell Medicine, en Nueva York, quien fue pionero en el uso de adenovirus como vectores, “y se ponen en sus genes”.
Los virus agregan naturalmente sus genomas a los de las células, lo que las induce a producir proteínas virales. En la década de 1990, investigadores agregaron genes a un adenovirus para producir una enzima que faltaba en un trastorno genético.
La idea era que las células infectadas produjeran la enzima, curando la enfermedad. En cambio, el primer paciente en ser tratado de esta manera murió de una reacción inmune severa.
“No nos dimos cuenta de cuán inmunogénicos eran estos virus”, dijo Crystal.
La trágica muerte fue un revés para la terapia génica, que solo revivió en los últimos años cuando se aprobaron varias terapias que podrían salvar vidas.
Mientras tanto, los desarrolladores de medicamentos y vacunas continuaron elaborando vacunas en torno a dosis mucho más pequeñas de adenovirus. Cuando se usa en cantidades más pequeñas, la reacción inmune al adenovirus “no es un problema”, según Crystal. En todo caso, los desarrolladores de vacunas ven la reacción inmune del cuerpo como una potencial ventaja, dijo.
“Actúan esencialmente como adyuvante, y eso amplifica la respuesta inmune” a la vacuna, dijo Crystal.
La inmunidad humana preexistente a los adenovirus de los chimpancés, como la que se usa en la vacuna de Oxford, es menos preocupante, dijo Lindsey Baden, especialista en enfermedades infecciosas en Brigham and Women’s Hospital, afiliado a Harvard, en un podcast patrocinado por el New England Journal of Medicine.
Con estas nuevas tecnologías, “la seguridad es difícil de conocer”, dijo Baden, quien ha trabajado en el campo de las vacunas contra el VIH durante décadas. “Si se ha estudiado en 1.000 personas, no se conoce el riesgo de 1 en 10.000; si se ha estudiado en 10.000 personas, no se conoce el riesgo de 1 en 100.000, y así sucesivamente”.
Si los adenovirus están asociados con los efectos secundarios que han aparecido en las vacunas contra el COVID, eso podría retrasar el desarrollo de una serie de proyectos, como sucedió con el VIH y la terapia génica. Hay más de una docena de vacunas contra el COVID en desarrollo basadas en adenovirus, según la Organizacion Mundial de la Salud.
*Tomado de El Financiero